Buckyballs: Nervenzellen müssen in den Käfig
Dieser Artikel ist älter als ein Jahr!
Viele Krankheiten gelten bis heute als unheilbar. Der Grund liegt oftmals an abgestorbenen oder etwa durch einen Unfall zerstörten Zellen oder am Nachlassen der Organfunktionen. Ein relativ junges Feld der Biomedizin – die Regenerative Medizin – kann hier vieles bewirken und erkranktes Gewebe erneuern und funktionstüchtig machen.
Generell befasst sie sich mit der Wiederherstellung von funktionsgestörten Zellen, Geweben oder Organen. „Dies geschieht entweder durch Anregung der körpereigenen Regenerations- und Reparaturprozesse oder aber durch biologischen Ersatz in Form von lebenden Zellen oder im Labor gezüchteten Geweben“, sagt Lars-Peter Kamolz, Leiter der klinischen Abteilung für Plastische, Ästhetische und Rekonstruktive Chirurgie an der Medizinischen Universität Graz.
Das Ziel sei ihm zufolge immer gleich: Möglichst den gesunden und funktionalen Originalzustand eines betroffenen Gewebes wiederherzustellen, anstatt es nur behelfsmäßig zu ersetzen und zu reparieren. „Heilen statt reparieren“ sei das Motto.
3D-Biodruck
Insbesondere der 3D-Biodruck hat das Feld revolutioniert. „Dank 3D-Drucktechniken können Zellen und Biomaterialien kombiniert und Schicht für Schicht abgeschieden werden, um biomedizinische Teile herzustellen, die die ,gleichen’ Eigenschaften wie natürliches Gewebe vorweisen“, sagt der Mediziner.
Der 3D-Druck kommt auch an der TU Wien zum Einsatz. Per sogenannter 2-Photonen-Polymerisation werden aktuell mikroskopisch kleine Käfige hergestellt, in die Nervenzellen hineingeschleust werden. Mithilfe eines fokussierten Laserstrahls werden bestimmte Stellen in einer Flüssigkeit ausgehärtet, wodurch dreidimensionale Gerüste, „ Buckyballs“ genannt, entstehen.

© TU Wien
Sie erinnern an winzige Fußbälle, bestehend aus Fünf- und Sechsecken mit kleinen Öffnungen. „Die Käfige sind dazu da, dass sich darin Zellen ansiedeln und Sphäroide formen“, sagt Aleksandr Ovsianikov, Leiter der Forschungsgruppe 3D-Printing and Biofabrication am Institut für Werkstoffwissenschaften und Werkstofftechnologie der TU Wien. Sphäroide sind kugelförmige Aggregate aus mehreren tausend Zellen.
Zellen folgen Schall
Um die Nervenzellen durch die Öffnungen in die Käfige zu bringen, wird eine neue Technologie der Stanford Universität eingesetzt, die mit der TU Wien zusammenarbeitet. In der Lösung, in der sich die Zellen befinden, werden akustische Schwingungen erzeugt. Laut Utkan Demirci, Co-Leiter des Canary Center at Stanford for Early Cancer Detection, folgen die Zellen den Schwingungen, „wie die Ratten in der Legende dem Rattenfänger von Hameln.“
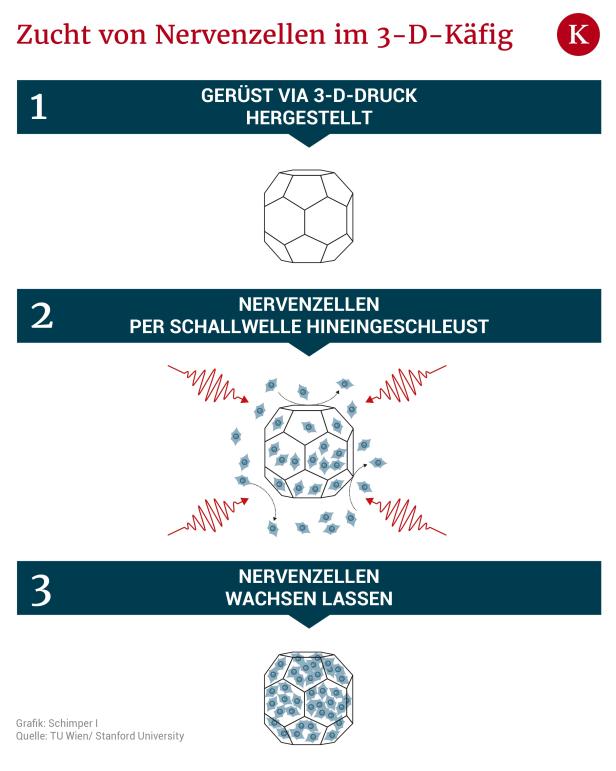
© Schimmer/TU Wien/ Stanford University
An bestimmten Punkten der Flüssigkeit bilden sich Schwingungsknoten, an denen die Flüssigkeit statisch ist. Dort werden die Zellen nicht mehr herumgewirbelt und bleiben haften. Und genau an diesen Knoten werden auch die Buckyballs platziert, in die die Zellen hineingeladen werden. So kann lebendiges Gewebe in einer bestimmten Form wachsen und das Zell-Verhalten manipuliert und gesteuert werden – etwa die Länge der Nervenverbindungen, die sich mit den benachbarten Buckyballs zusammenschließen. Die Gerüststrukturen könnten auf diese Weise viel dichter und effizienter beladen werden, als es mit herkömmlichen Methoden der Zellbesiedelung überhaupt möglich wäre.
Für die Studie wurden mehrere Designs erzeugt: „Wir wollen wissen, bei welchen Käfigen mehrere Zellen zurückbleiben, damit man sieht, wie effizient man diese befüllen kann“, so Ovsianikov. Auch sei es wichtig herauszufinden, wie die Zellen kommunizieren und welche Rolle die Abstände zwischen den Käfigen und die Anzahl der Zellen spielen. Mithilfe der so erzeugten neuronalen Netzwerke ließen sich in Zukunft jedenfalls biologische Fragen klären, auf die man sonst experimentell keinen direkten Zugang hätte.
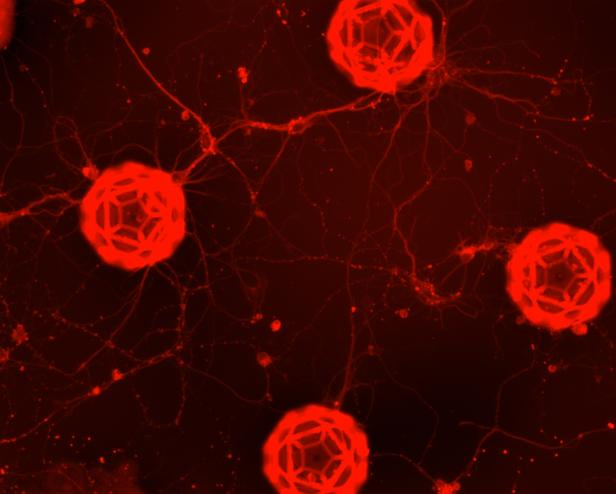
Über die Nervenverbindungen schließen sich alle benachbarten Buckyballs zusammen
© Stanford University
Einsatz bei Menschen
Wiederhergestelltes Gewebe und sogar einzeln erneuerte Nerven kommen aber heute schon zur Anwendung. „Hauptindikationen für sogenannte ,Nervenrekonstruktionen’ stellen Unfälle dar, sowie Nervenrekonstruktionen und der Einsatz nach Tumoroperationen“, erklärt der Mediziner Lars-Peter Kamolz. Aufgrund der begrenzten Verfügbarkeit von Spendernerven konzentriere sich die Forschung im Bereich des „Neural Tissue Engineering“ vorrangig auf die Entwicklung bioartifizieller Nervenführungskanäle. „Ähnliche Techniken werden auch für die Nervenreparatur bzw. Nervenregeneration im Rückenmark untersucht und entwickelt“, sagt er.
Entscheidend für das Funktionieren dieser Kanäle seien jedenfalls die Struktur der verwendeten Buckyballs, das Gerüstmaterial und ob die Gerüste mit Zellen besiedelt oder etwa mit Wachstumsfaktoren (Proteine) beschichtet werden, die die Nervenregeneration fördern sollen. Durch innovative Ansätze der Regenerativen Medizin besteht aber auch die Hoffnung, dass in Zukunft Krebs- und Herzerkrankungen und neuronale Krankheiten wie Morbus Parkinson oder Querschnittlähmungen geheilt werden können.
Biologisch abbaubar
Um erneuerte Zellen, Organe und Gewebe beim Menschen einsetzen zu können, müssen erst Mikrokäfige („Buckyballs“) hergestellt werden, in die – je nach Gebrauch – unterschiedliche Zellen geschleust werden. Dort können sie sich miteinander verbinden und lebendiges Gewebe kann wachsen.
Wesentlich dabei ist die biologische Abbaubarkeit der Buckyballs: „Denn nach dem Einsetzen in den menschlichen Körper sollen die Gerüste nicht ewig dort bleiben“, sagt Olivier Guillaume vom Institut für Werkstoffwissenschaften und Werkstofftechnologie der TU Wien.
Käfig aus Hydrogel
Die Gerüste können etwa aus plastikähnlichen Materialien oder aus Hydrogel hergestellt werden, das sich grundsätzlich besser eignet. Hydrogel ist ein Wasser enthaltendes, aber wasserunlösliches Polymer. In diese Gerüste werden im Rahmen eines aktuellen Forschungsprojekts der TU Wien Fettstammzellen integriert.
So wachsen sie zu sogenannten Sphäroiden, also Anhäufungen aus tausenden Zellen, zusammen, die dem Menschen später injiziert werden können, sodass sich zerstörtes Knorpel- oder Knochengewebe regenerieren kann. „Mithilfe unserer Buckyballs aus Polymeren können sie besser und länger haften bleiben, sodass die Zellen Zeit haben, das Gewebe von selbst wiederaufzubauen. Danach benötigen sie keine Unterstützung mehr – die Buckyballs werden vom Körper abgebaut,“ erklärt der Forscher.


Kommentare