Zusätzliche DNA-Buchstaben ermöglichen neue Chemie
Dieser Artikel ist älter als ein Jahr!
"Zumindest seit dem letzten gemeinsamen Vorfahren aller Lebensformen auf der Erde wird genetische Information in einem Alphabet aus vier Buchstaben gespeichert, das durch die Bildung zweier Basenpaare ausgelesen und weitergegeben wird", heißt es in einer kürzlichen Veröffentlichung im Fachmagazin Nature. Das ist nicht länger der Fall.
Den Forschern, die an der Publikation beteiligt waren, ist es nämlich gelungen, einen Organismus zu schaffen, der ein ABC aus sechs Buchstaben nutzt. Neben den Basenpaaren GA (Guanin-Adenin) und CT (Cytosin-Thymin) verfügt dessen DNA auch noch über das Duo XY (dNaM–dTPT3). Im Gegensatz zu ähnlichen Versuchen in der Vergangenheit nutzen die von den Wissenschaftlern modifizierten Escherichia coli Bakterien ihr zusätzliches Basenpaar, um Proteine zu erzeugen, die ihre natürlichen Verwandten nicht im Repertoire haben.
Heiliger Gral für Forschung
Neben den 20 Aminosäuren, die in der Natur von Lebewesen genutzt werden, können die semisynthetischen Bakterien mit dem zusätzlichen Informationsgehalt ihrer DNA für weitere Aminosäuren codieren. Diese können dann in den Ribosomen zu Proteinen zusammengesetzt werden, die in der Natur nicht vorkommen. Die im Nature-Artikel beschriebenen Bakterien führen ein normales Bakterienleben, produzieren aber ein fluoreszierendes Protein, das kein natürlicher Organismus synthetisieren kann.
Die Herstellung neuer, maßgeschneiderter Proteine ist für die Forschung ein heiliger Gral. Sie könnten als Katalysatoren dienen, um chemische Reaktionen nach Wunsch ablaufen zu lassen oder als Medikamente gegen diverse Krankheiten eingesetzt werden.
Die futurezone hat den Nature-Coautor Floyd Romesberg vom Scripps Research Institute gefragt, wo das größte Potenzial liegt, warum die Natur sich auf vier Buchstaben festzulegen scheint und ob auch Menschen mit zusätzlichen Basen denkbar wären.
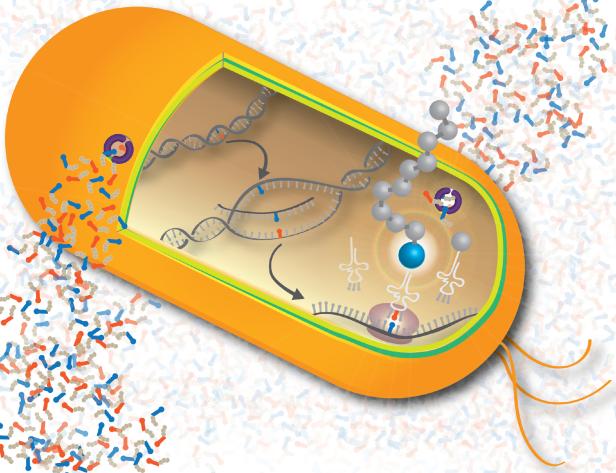
© Jodie Chin, Scripps Research

© Romesberg Lab
futurezone: Warum besteht alle DNA in der Natur aus zwei Basenpaaren?
Floyd Romesberg:Forscher diskutieren darüber, seit die Struktur der DNA vor mehr als 60 Jahren beschrieben wurde. Die Frage ist aber unmöglich zu beantworten, weil wir nicht wissen, unter welchen Bedingungen sich das Leben entwickelt hat. Unsere Arbeit erlaubt uns zu prüfen, ob es Bedingungen geben könnte, unter denen die höhere Komplexität zusätzlicher Basenpaare ein Vorteil wäre. Wir statten Zellen mit drei Basenpaaren aus und sehen, was passiert, wenn statt dem natürlichen 20 jetzt 21, 22, oder 25 Aminosäuren zur Verfügung stehen. Die veränderten Zellen können wir dann mit ihren natürlichen Pendants vergleichen.
Könnte es sein, dass die Evolution einfach deshalb bei zwei Basenpaaren geblieben ist, weil höhere Komplexität die Fehleranfälligkeit steigen lässt?
Es kann sein, dass durch den höheren Aufwand bei der Speicherung und Bearbeitung genetischer Information mit drei Paaren ein Nachteil für Organismen entsteht. Vielleicht lohnt sich der höhere Aufwand auf Dauer einfach nicht. Dafür erhöht die komplexere Variante die verfügbare Informationsmenge deutlich. Es gibt aber auf jeden Fall eine Obergrenze, ab der sich das nicht mehr rechnet. Bei 20 Basenpaaren, die in Schuss gehalten werden müssen, wäre schon das Kopieren der Information eine Herausforderung.
Unterscheiden sich die Bakterien mit zusätzlichen Nukleotiden von ihren natürlichen Verwandten?
Es gibt praktisch keine Unterschiede zwischen unseren Zellen und ihren natürlichen Verwandten. Sie wachsen geringfügig langsamer, aber der Unterschied ist kleiner als zwischen verschiedenen Bakterienstämmen. Unsere semisynthetischen Bakterien sehen unter dem Mikroskop ganz normal aus.
© Scripps Research
Könnten die modifizierten Bakterien in der Natur überleben?
In der Natur könnten sie sich nicht vermehren, weil sie die zusätzlichen, nicht natürlichen Basen, die wir mit X und Y abkürzen, nicht selbst herstellen können. Wir müssen sie künstlich zuführen.
Laut Jurassic Park findet das Leben doch immer einen Weg.
Sie könnten sich irgendwann so weiterentwickeln, dass sie auch X und Y herstellen könnten. Das ist aber etwa so, wie wenn ich sage, dass ich eine Möglichkeit finden könnten, ohne Hilfsmittel zum Mond zu fliegen. Die Bakterien müssten für die Herstellung von X und Y jeweils einen neuen Prozess mit 10 bis 15 Schritten entwickeln, für den sie nicht einmal die Grundvoraussetzungen haben. So funktioniert Biologie nicht, hier wird vorhandenes in kleinen Schritten abgewandelt.
Wird das zusätzliche Basenpaar stabil vererbt?
Unsere semisynthetischen Organismen verlieren ihre Fähigkeit mit der Zeit. Für wie viele Teilungsvorgänge das anhält, ist unterschiedlich. Wir haben aber bereits eine Methode entwickelt, die verhindert, dass die Änderungen im Genom revertieren. Das werden wir in Kürze veröffentlichen.
Haben Sie auch schon versucht, vier Basenpaare zu realisieren?
Wir haben zwei neue Basen, die wir mit X und Y abkürzen, hinzugefügt, also ein zusätzliches Basenpaar. Ich glaube, es wäre möglich weitere hinzuzufügen, allerdings nicht mit unserem Ansatz. Die natürlichen Vertreter Guanin, Cytosin, Adenin und Thymin nutzen Wasserstoffbrücken für die Basenpaarbindung. Wir nutzen für das zusätzliche Paar Hydrophobie, um die Bindung herzustellen. So verhindern wir, dass X und Y sich mit G, C, A oder T verbinden. Sie können also nur miteinander ein Paar bilden. Weitere Nukleinbasen auf dieser Grundlage hinzuzufügen, könnte zu ungewollten Verbindungen mit X oder Y führen. Wir haben vor allem bewiesen, dass jeder Schritt in der Zelle auch ohne Wasserstoffbrücken funktioniert. Das war eine Machbarkeitsstudie.
Wie viele zusätzliche Aminosäuren ergeben sich durch das künstliche Basenpaar?
Information wird erst durch die Umschrift von DNA in tRNA nutzbar gemacht. Diese RNA wird in Codons geschrieben. Die kann man sich als Wörter aus drei Buchstaben vorstellen. Dadurch stehen in einem natürlichen Organismus 4x4x4 Wörter zur Verfügung, die für Aminosäuren codieren könnten, das wären 64 Aminosäuren. Allerdings sind drei Wörter Stoppsignale, die das Ende eines Gens kennzeichnen. Bleiben 61 theoretisch mögliche Aminosäuren, von denen aber nur 20 tatsächlich vorkommen. Das liegt daran, dass es eine Menge Synonyme in diesem Wörterbuch gibt. Mit einem künstlichen Basenpaar erhöht sich die Zahl der möglichen Codons auf 6x6x6, also 216. Das heißt aber nicht, dass wir 152 zusätzliche Aminosäuren bekommen. Wir können derzeit nur drei bis vier neue Aminosäuren nutzen, zwei davon wirklich gut. Das technische Limit liegt wohl bei fünf bis sechs.
Was bedeutet das für die Zahl der möglichen neuen Proteine?
Schon unsere zwei vielversprechendsten neuen Aminosäuren erlauben eine riesige Anzahl neuer Proteine. Deshalb sind wir auch nicht darauf aus, die Zahl der Aminosäuren weiter zu erhöhen. Wir wollen jetzt das Potenzial der Proteine ausschöpfen.
Wie genau lässt sich ein gewünschtes Protein planen, etwa um einen maßgeschneiderten Katalysator zu bekommen?
Wir können einer Zelle sagen, welches Protein sie machen soll. Das Problem ist, dass wir oft nicht wissen, was wir wollen. Wir wissen zum Beispiel nicht genug darüber, wie Proteine als Katalysatoren funktioniert. Allerdings hat die Biologie den Vorteil, dass wir bei der Proteinsynthese auch die Evolution nutzen können. Wir können unsere Zellen so designen, dass sie möglichst nahe am gewünschten Ergebnis operieren und sie sich dann weiterentwickeln lassen. Es wird noch eine Weile dauern, bis wir auf diesem Gebiet Anwendungen sehen.
Wo gibt es sonst praktisches Potenzial?
Einfacher als bei Proteinen ist die Sache bei proteinbasierten Medikamenten (das wohl bekannteste ist Insulin, Anm.). Hier können wir recht genau sagen, wie das Ergebnis der Synthese aussehen soll und das praktisch am Reißbrett entwerfen. Das ist eine große Sache. Allerdings muss das gewünschte Protein nicht nur an der gewünschten Stelle im Körper andocken können, sondern auch stabil bleiben und darf nicht sofort wieder abgebaut werden. Ich kann also sagen, ich brauche an dieser und jener Stelle im Protein ein Lipid, damit es nicht zu schnell gefiltert wird.
Wie weit ist eine Anwendung hier noch entfernt?
Ich habe 2014 eine Biotechnologiefirma gestartet, die auf solche Medikamente spezialisiert ist. Wir wollen in sechs bis acht Monaten erste brauchbare Proteine liefern. Das Einfügen eines Lipids in ein Protein ist einfach. Wir wollen möglichst bald Anwendungen liefern, unsere Arbeit soll nicht in Schubladen versauern.
Wie sehen Ihre nächsten Ziele aus?
Wir wollen die Zahl der neuen Aminosäuren auf fünf bis sechs erhöhen. Zudem werden wir Anwendungen in der Biotechnologie entwickeln. In einem weiteren Schritt möchten wir auch höhere Zellen, etwa Hefe oder menschliche Zellen, mit neuen Basenpaar ausstatten. Langfristig wollen wir auch wissen, was passiert, wenn wir höhere Organismen mit zusätzlichen Basen ausstatten. Das wird am Anfang der Fadenwurm C. Elegans sein. Dann können wir sehen, ob sich die modifizierten Tiere von ihren natürlichen Verwandten unterscheiden, ob sie schneller kriechen oder andere Unterschiede vorhanden sind. Da sind wir auf der Zellebene heute noch stark eingeschränkt.
Wie lange wird es dauern, bis höhere Organismen mit zusätzlichen Nukleotiden erschaffen werden?
C.elegans werden wir wohl in fünf Jahren haben. Bei komplexeren Organismen wie Fruchtfliegen wird es schwieriger, da wir X und Y in jede Zelle bringen müssen. Es wäre vielleicht denkbar, ein Tier zu schaffen, das das zusätzliche Basenpaar nur in der Haut trägt.
Wäre ein Mensch mit zusätzlichen Nukleotiden denkbar?
Ein Versuch an Menschen wäre theoretisch denkbar, aber daraus ergäben sich eine Vielzahl von ethischen Problemen. Da stellt sich wie so oft die Frage, ob man etwas, nur weil man kann, auch wirklich machen soll.
Kommentare