Impfstoff aus Deutschland zeigt positive Wirkung in ersten Tests
Dieser Artikel ist älter als ein Jahr!
Auf der Suche nach einem Impfstoff gegen das neue Coronavirus sind das Mainzer Biopharma-Unternehmen Biontech und der US-Konzern Pfizer zumindest einen gewissen Schritt vorangekommen. Bei Tests in den USA entwickelten Probanden wirksame Antikörper gegen den Erreger Sars-CoV-2. Das teilten Biontech und Pfizer am Mittwoch gemeinsam mit. Unklar ist noch, ob diese Antikörper tatsächlich vor einer Infektion mit Sars-CoV-2 schützen. Das sollen nun Tests mit bis zu 30.000 Probanden zeigen.
Mehrere Experten bewerteten die Ergebnisse positiv. Der Immunologe Bernhard Fleischer, ehemaliger Direktor des Bernhard-Nocht-Instituts für Tropenmedizin, sagte, die Ergebnisse seien „sehr bemerkenswert“. Er würde davon ausgehen, mit dem Impfstoff vor einer Infektion mit dem Coronavirus geschützt zu sein. Erwiesen sei das aber noch nicht.
Die bereits erfolgten Tests in den USA umfassten 45 gesunde Probanden im Alter von 18 bis 55 Jahren. 24 davon bekamen je zwei Injektionen des Wirkstoffs - einige in etwas höherer Dosis. Zwölf Probanden erhielten letztlich nur einmal eine hohe Dosis, dieser Ansatz wurde aber nicht weiter verfolgt. Hinzu kam eine neunköpfige Kontrollgruppe, die zwei Dosen Placebo bekam. Sofern zwei Dosen verabreicht wurden, geschah dies im Abstand von drei Wochen.
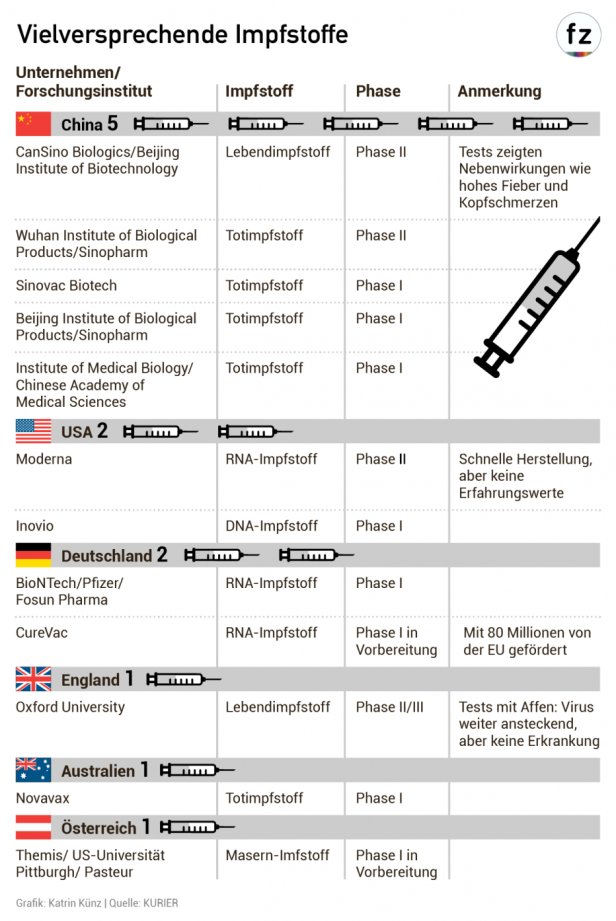
© Kurier Grafik
Nach der Impfung haben sich Antikörper gebildet
Sieben Tage nach der zweiten Impfung wurden bei allen 24 Probanden mit zwei Impfungen Antikörper festgestellt, die das Virus Sars-CoV-2 in einem anschließenden Labortest ausschalten konnten. Diese Menschen zeigten auch eine deutlich stärkere Antikörperbildung als Menschen, die bereits mit Sars-COV-2 infiziert waren. Abhängig von der Impfstoff-Dosis hatten die Geimpften 1,8 oder 2,8 Mal mehr neutralisierende Antikörper gegen das Coronavirus gebildet.
Zu schwerwiegenden Nebenwirkungen kam es den Angaben von Biontech und Pfizer zufolge nicht, bei den Kandidaten mit zwei Impfungen seien lediglich „milde bis moderate lokale und systemische Reaktionen“ zu beobachten gewesen. Die am häufigsten vorkommende lokale Reaktion sei ein Schmerz an der Einstichstelle gewesen.
„Das sind ganz gute Signale“, kommentiert Stephan Becker, Virologe an der Uni Marburg. Insbesondere sei gut, dass die Antikörperkonzentration höher sei als bei Menschen, die eine Infektion durchgemacht haben. Ob der Impfstoffkandidat tatsächlich vor einer Infektion schützt, zeigten die Ergebnisse aber nicht, sagte Becker. Zudem sei unklar, ob die Impfung zum Aufbau eines sogenannten Immungedächtnisses führt, also dass der Körper auf eine Infektion mit dem Coronavirus wirksam vorbereitet ist.
Um das zu zeigen, müssen viele Tausend Menschen geimpft werden, um dann zu schauen, wie viele von ihnen sich unter realen Bedingungen mit dem Coronavirus infizieren. Becker ist an den Corona-Projekten von Biontech nicht beteiligt, kooperiert aber mit der Firma bei anderen Projekten.
Ermutigende Ergebnisse
„Daten zur Immunantwort nach Impfung beim Menschen sind tatsächlich ein wichtiger und ermutigender Schritt auf dem Weg zu einem Impfstoff“, sagte der Präsident des Paul-Ehrlich-Instituts, Klaus Cichutek. Das gelte insbesondere bei einem RNA-Impfstoff wie diesem, denn es gebe noch keine solchen zugelassenen Human-Impfstoffe, und es sei weltweit auch wenig Erfahrung mit „präventiven RNA-Impfstoffen“ da.
Vor Biontech und Pfizer habe das Biotech-Unternehmen Moderna aus den USA die Induktion einer Immunantwort beim Menschen durch einen RNA-Impfstoffkandidaten bekanntgegeben. Dafür habe es nun also den weltweit zweiten Hinweis gegeben.
Biontech-Mitbegründer und -Chef Ugur Sahin nannte die vorläufigen Daten sehr ermutigend. Sie zeigten, dass der Impfstoffkandidat „eine Immunantwort mit neutralisierenden Antikörpern im Menschen induzieren kann“. „Wir freuen uns darauf, zusätzliche Daten zu BNT 162b1 zu veröffentlichen“, sagte er. Biontech testet potenzielle Impfstoffe auch in Deutschland. Es hatte hierzulande als erstes Unternehmen die Genehmigung des Paul-Ehrlich-Instituts bekommen. BNT 162b1 ist der Name des Impfstoffkandidaten, zu dem nun die US-Ergebnisse vorliegen. Kathrin U. Jansen, Senior Vice President bei Pfizer und für die Impfstoffforschung zuständig, sagte, die ersten klinischen Daten stimmten zuversichtlich.
Weitere Tests notwendig
Mit den bereits erfolgten und sich nun anschließenden Tests wollen Biontech und Pfizer die richtige Dosis für einen möglichen Impfstoff herausfinden. Es muss auch eine Auswahl getroffen werden, mit welchen Impfstoffkandidaten in einer großangelegten, globalen Studie mit über 30.000 gesunden Probanden gearbeitet wird. Die könnte - sofern sie von den Behörden genehmigt wird - im späten Juli 2020 beginnen.
Noch sei BNT 162b1 in keinem Land der Welt für den Gebrauch zugelassen, betonten Biontech und Pfizer. Sollte der Impfstoff aber zugelassen werden, planen die Firmen, bis Ende dieses Jahres bis zu 100 Millionen Impfstoffdosen und bis Ende kommenden Jahres möglicherweise mehr als 1,2 Milliarden Dosen herstellen zu können.

Kommentare