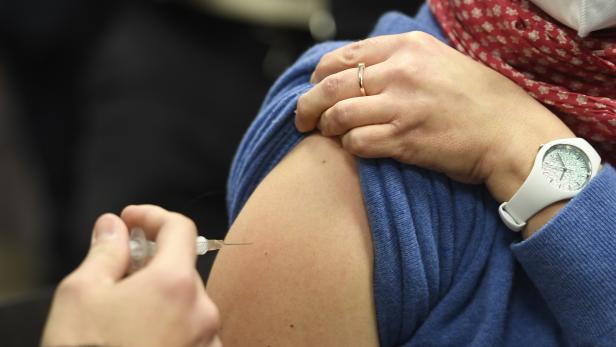
Neuer Corona-Impfstoff aus Österreich könnte vor Omikron schützen
Dieser Artikel ist älter als ein Jahr!
Ein an der Medizinischen Universität Wien (MedUni) entwickelter Impfstoff gegen das Corona-Virus hat in präklinischen Daten gezeigt, dass er gegen alle bisher bekannten SARS-CoV-2-Varianten inklusive Omikron wirken kann und zwar auch bei Menschen, die bisher keinen Impfschutz (Non-Responder) aufgebaut haben, hieß es in einer Aussendung am Dienstag.
Mischung aus Corona- und Hepatitis B-Impfstoff
Es handelt sich um eine Kombination aus Corona- und Hepatitis B-Impfstoff. Die Studie wurden im Magazin „Allergy“ veröffentlicht. Der an der MedUni Wien unter Studienleitung von Rudolf Valenta vom Zentrum für Pathophysiologie, Infektiologie und Immunologie entwickelte Antigen-basierte Impfstoff zielt auf die Rezeptorbindungsdomänen (RBD) des SARS-CoV-2 Virus ab und regte im Tiermodell und im humanen Test eine robuste und einheitliche RBD-spezifische IgG-Antikörperreaktion an. Durch diese Antikörperreaktion wird das Andocken und Eindringen des Virus in die Körperzellen verhindert, sodass es zu keiner Infektion kommt.
Impfstoff induziert langlebige Antikörper
Der an der MedUni Wien entwickelte SARS-CoV-2-Subunit-Impfstoff (PreS-RBD) basiert auf einem strukturell gefalteten künstlich hergestellten Protein, das aus zwei Rezeptorbindungsdomänen (RBD) des SARS-CoV-2 Virus und dem PreS Antigen aus Hepatitis B, die als immunologische Träger füreinander dienen und damit die Immunantwort verstärken. Derzeit verfügbare genetische SARS-CoV-2-Impfstoffe induzieren hauptsächlich vorübergehende IgG1-Antikörper Antworten, während der PreS-RBD-Impfstoff zusätzlich auch langlebige RBD-spezifische IgG4-Antikörper induzieren kann.
Die im Blut und Schleimhautsekreten nachgewiesenen PreS-RBD-spezifischen IgG-Antikörper reagierten mit SARS-CoV-2-Varianten, einschließlich der Omikron-Variante. Die durch Impfung mit PreS-RBD induzierten Antikörper hemmten die Bindung von RBD mit seinem menschlichen Rezeptor ACE2 stärker, und ihre virusneutralisierenden Titer waren höher als jene in einer Zufallsstichprobe von Personen, die vollständig mit zwei Teilimpfungen von derzeit registrierten Impfstoffen immunisiert worden waren, oder als jene von COVID-19-Rekonvaleszenten (d.h. ehemals an COVID-19 erkrankten Personen).
Wirkung auch bei "Non-Respondern"
„Der PreS-RBD-Impfstoff hat das Potenzial, eine sterilisierende Immunität gegen alte und neue SARS-CoV-2 Varianten zu erzielen, indem er durch die Hemmung des zellulären Viruseintritts die Infektion verhindert, sodass es auch zu keiner Virusproduktion und Weitergabe mehr kommt“, erklärte Studienleiter Rudolf Valenta.
Außerdem wird erwartet, dass der Impfstoff auch bei Menschen wirkt, die bisher nicht auf Impfungen angesprochen haben („RBD non-responder“), da sie durch den PreS Anteil des Impfstoffes eine zusätzliche T-Zell-Hilfe bekommen. Eine frühere Studie von Valenta und seinen Kollegen hatte ergeben, dass circa 20 Prozent der von der COVID-19 Erkrankung Genesenen keine RBD-spezifischen Antikörper bilden konnten und somit einem ständigen Risiko der Re-Infektion ausgesetzt waren.
Inspiration von Allergieimpfstoffen
Die Entwicklung dieses österreichischen Corona-Impfstoffes wurde stark durch die jahrzehntelange Erfahrung in der Konstruktion von Allergieimpfstoffen inspiriert, hieß es in der Aussendung. Frühere Arbeiten über Allergieimpfstoffe und klinische Studien, die auch mit PreS-basierten Allergieimpfstoffen durchgeführt wurden, haben die Sicherheit der PreS-basierten Impfstoffes gezeigt, auch wenn sie wiederholt angewendet werden.
„Unsere Daten lassen hoffen, dass dieses leicht herstellbare Eiweiß-basierte Impfantigen gegen alle bisher bekannten SARS-CoV-2 Varianten inklusive Omikron wirken wird“, sagte Studienleiter Rudolf Valenta. „Der Impfstoff ist darauf ausgelegt, wiederholte Injektionen zum Aufbau einer nachhaltigen sterilisierenden Immunität möglich zu machen, könnte in allen Alters- und Risikogruppen zum Einsatz kommen und scheint den bisher erhältlichen Impfstoffen bezüglich der Induktion neutralisierender Antikörper überlegen zu sein.“
Wenn ausreichend finanzielle Mittel eingesetzt werden, könnten die ersten klinischen Studien, die für eine Zulassung nötig sind, noch in diesem Jahr durchgeführt werden, hieß es.

Kommentare